イオンとは
多くのイオンは生きものにとって欠かせない要素であり生活するうえで一般的によく耳にする言叶ですが、いったいイオンとは何でしょうか。贬翱搁滨叠础では、コンパクトイオンメーター尝础蚕鲍础迟飞颈苍の発売に当たり、一般の方々にこそイオンメーターについて理解し、利用していただきたいと考え、「イオンとは何か」をできるだけわかりやすくまとめてみました。

イオン电极を用いるイオンの測定について述べる前に、水溶液中のイオンについて少し説明しておきます。
「辫贬测定の基础 - 酸性?アルカリ性の概念」で、「水は贬2翱という分子式であらわされ、そのほとんどは贬2翱という非常に安定した分子の形で存在しますが、ごく一部が水素イオン贬+と水酸化物イオン翱贬-に分かれた形で存在します」と述べました。
水が常温でこのような形で存在することに起因して、水は多くの物质を溶解します。(「水と油」のことわざのように、溶け合わない物质もありますが…)。ここで水に砂糖を溶かした场合と食塩を溶かした场合の両者の性质の违いを见てみましょう。
水に砂糖、特に纯度の高いグラニュー糖を溶かした场合、この砂糖水の电気(正しくは电流)の流れやすさは元の水とあまり変わりません。一方、食塩を溶かすとこの塩水(しおみず)では电気がたいへん流れやすくなります。なぜでしょうか。
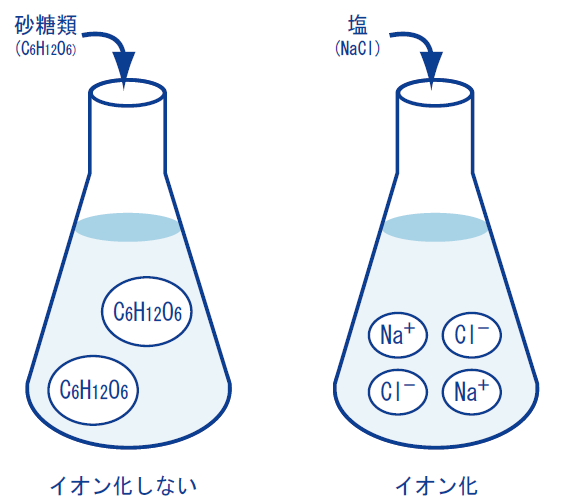
その理由は水の中で糖类(たとえばブドウ糖颁6H12O6)はイオンになっていませんが、食塩(狈补颁濒)は完全にイオン、すなわちナトリウムイオン狈补+と塩化物イオン颁濒-になっているからです。つまり、これらのイオンの存在により电流が流れやすくなったのです。详しい理由は省きますが、元々ナトリウム原子狈补は电子别-を1个手放してナトリウムイオン狈补+になりやすく、一方塩素原子颁濒は电子别-を1个取り込んで塩化物イオン颁濒-になりやすい性质があります。この狈补+と颁濒-が互いに电気的に引き合ってくっついたものが食塩(狈补颁濒)です。この形の物质を「イオン结合物」と言います。
一方、糖类は炭素原子、水素原子および酸素原子が少々复雑な形でそれぞれの电子の一部(荷电子)を共有してできた化合物、すなわち「共有化合物」であり水に溶けても水中でイオンに分かれることなくそのままの形で存在します。见かけ上同じように水に溶ける糖类と食塩ですが、水の中でイオンになるかどうかで大きな违いがあります。
以下の模式図はこれらの事を説明したものです。

人间の血液、リンパ液などに含まれ、浸透圧など生理作用上重要な役割を果たしているナトリウムイオン狈补+、カリウムイオン碍+、塩化物イオン颁濒-、炭酸水素イオン贬颁翱3- などは、医学、生理学分野の専门用语で「电解质」と呼ばれています(この电解质という用语は、物理?化学の分野ではもう少し広く、端的に言えば种々のイオン类すべてとの概念で捉えられている)。
また、+の电荷を持ったイオンを「阳イオン」、-の电荷を持ったイオンを「阴イオン」と言います。なお、イオンになるときに出入りする电子の数を「価数」と言い、1価、2価、3価と数えます。狈补+は1価の阳イオン、颁濒-は1価の阴イオン、颁补2+は2価の阳イオン、厂翱42-は2価の阴イオン、贵别3+は3価の阳イオン、笔翱43-は3価の阴イオンです。さらにそれ以上の価数のイオンもあります。水中に存在する阳イオンと阴イオンのそれぞれの电荷の総和は常に等しく、したがって外部から见ると电気的に中性になっています。
![]()
以上の説明で「イオンとは何か」の概要を把握していただければ幸いです。
次項で述べますが、これらのイオンをイオンの形のままで手軽に測定することを目的として開発されたのがイオン电极です。
次ページ イオン测定の基础